Answer:
B. 2 litros.
Step-by-step explanation:
De acuerdo con el enunciado, el gas experimenta un proceso isotérmico y se conserva su masa. Asumiendo que el gas se comporta idealmente, tenemos la siguiente relación entre los estados final e inicial:
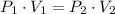 (1)
(1)
Donde:
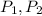 - Presiones inicial y final, medidos en atmósferas.
- Presiones inicial y final, medidos en atmósferas.
 - Volúmenes inicial y final, medidos en litros.
- Volúmenes inicial y final, medidos en litros.
Si sabemos que
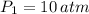 ,
,
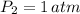 y
y
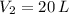 , entonces el volumen inicial del gas es:
, entonces el volumen inicial del gas es:
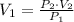

Por lo tanto, la respuesta correcta es B.