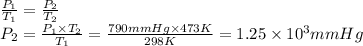Respuesta:
1.25 × 10³ mmHg
Explicación:
- Presión inicial (P₁): 790 mmHg
- Temperatura inicial (T₁): 25 °C
- Temperatura final (T₂): 200 °C
Paso 1: Convertir las temperaturas a Kelvin
Cuando trabajamos con gases ideales debemos convertir las temperaturas a Kelvin. Usaremos la siguiente ecuación:
K = °C + 273.15
K = 25°C + 273.15 = 298 K
K = 200°C + 273.15 = 473 K
Paso 2: Calcular la presión final
Usaremos la ley de Gay-Lussac.