Answer:
La densidad del tetracloruro de carbono es 1.990 gramos por centímetro cúbico.
Step-by-step explanation:
La masa de agua contenida dentro de la botella es igual a la diferencia entre la masa pesada totalmente llena y la masa pesada totalmente vacía, es decir:
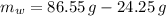
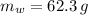
Ahora, de acuerdo con la definición de densidad, la masa es directamente proporcional a la densidad, entonces, podemos calcular la densidad del solvente mediante la siguiente relación:
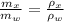 (1)
(1)
Donde:
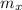 - Masa del tetracloruro de carbono, en gramos.
- Masa del tetracloruro de carbono, en gramos.
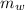 - Masa del agua, en gramos.
- Masa del agua, en gramos.
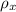 - Densidad del tetracloruro de carbono, en gramos por centímetro cúbico.
- Densidad del tetracloruro de carbono, en gramos por centímetro cúbico.
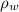 - Densidad del agua, en gramos por centímetro cúbico.
- Densidad del agua, en gramos por centímetro cúbico.
Si sabemos que
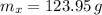 ,
,
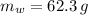 y
y
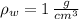 , entonces la densidad del tetracloruro de carbono es:
, entonces la densidad del tetracloruro de carbono es:
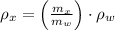
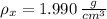
La densidad del tetracloruro de carbono es 1.990 gramos por centímetro cúbico.